Thu hồi, đình chỉ lưu hành bột khử mùi Trapha chai 30g
Cụ thể, Cục Quản lý Dược (Bộ Y tế) ra thông đình chỉ lưu hành, thu hồi và tiêu hủy trên toàn quốc sản phẩm Bột khử mùi Trapha loại hộp 1 chai 30g (Số lô: 2823; NSX: 18/9/23; HSD: 18/9/26; Số công bố: 01/19/CBMP-TNg).
Đơn vị chịu trách nhiệm đưa sản phẩm ra thị trường: Công ty Cổ phần Traphaco (địa chỉ: Số 75 Yên Ninh, quận Ba Đình, TP Hà Nội); Công ty cổ phần dược và vật tư y tế Thái Nguyên (địa chỉ: Số 477 Lương Ngọc Quyến, phường Phan Đình Phùng, TP Thái Nguyên) sản xuất.
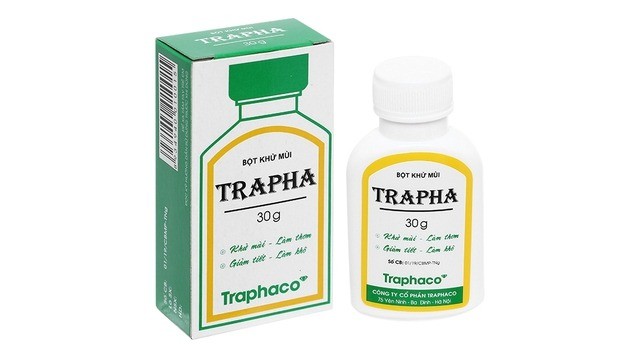 |
| Sản phẩm bột khử mùi Trapha 30g bị đình chỉ lưu hành, thu hồi và tiêu hủy trên toàn quốc. |
Lý do thu hồi mẫu kiểm nghiệm không đạt tiêu chuẩn chất lượng về chỉ tiêu giới hạn kim loại nặng.
Cục Quản lý Dược đã đề nghị Sở Y tế các tỉnh, thành phố trực thuộc Trung ương thông báo cho các cơ sở kinh doanh, sử dụng mỹ phẩm trên địa bàn ngừng ngay việc kinh doanh, sử dụng lô sản phẩm bột khử mùi Trapha loại hộp 1 chai 30g nêu trên và trả lại cơ sở cung ứng sản phẩm; tiến hành thu hồi lô và tiêu hủy lô sản phẩm vi phạm nêu trên; kiểm tra, giám sát các đơn vị thực hiện thông báo này; xử lý các đơn vị vi phạm theo quy định hiện hành.
Công ty cổ phần Traphaco, Công ty Cổ phần Dược và vật tư y tế Thái Nguyên phải gửi thông báo thu hồi tới những nơi phân phối, sử dụng lô sản phẩm bột khử mùi Trapha loại hộp 1 chai 30g nêu trên; tiếp nhận sản phẩm trả lại từ các cơ sở kinh doanh và tiến hành thu hồi, tiêu hủy toàn bộ lô sản phẩm không đáp ứng quy định.
Các đơn vị gửi báo cáo thu hồi và tiêu hủy lô sản phẩm bột khử mùi Trapha - hộp 1 chai 30g nêu trên về Cục Quản lý Dược trước ngày 5/4/2024.
Đồng thời, Cục Quản lý Dược cũng đề nghị Sở Y tế TP Hà Nội, Sở Y tế tỉnh Thái Nguyên kiểm tra Công ty Cổ phần Traphaco, Công ty Cổ phần Dược và vật tư y tế Thái Nguyên trong việc chấp hành các quy định của pháp luật về quản lý mỹ phẩm trong hoạt động sản xuất, kinh doanh mỹ phẩm.
Các đơn vị giám sát các công ty thực hiện thu hồi và tiêu hủy lô sản phẩm bột khử mùi Trapha loại hộp 1 chai 30g không đáp ứng quy định; xử lý, xử phạt vi phạm theo quy định hiện hành và báo cáo kết quả về Cục Quản lý Dược trước ngày 20/4/2024.
Tin liên quan
Cùng chuyên mục
Đọc thêm
 Tin Y tế
Tin Y tế
Việt Nam chủ động ứng phó với nguy cơ dịch bệnh Chikungunya
 Tin Y tế
Tin Y tế
Tăng cường phòng, chống bệnh Chikungunya
 Nhịp sống phương Nam
Nhịp sống phương Nam
TP Hồ Chí Minh hoàn tất việc đổi tên 26 bệnh viện công lập
 Tin Y tế
Tin Y tế
Hà Nội: Ngành Y tế sẵn sàng cho đêm hội Tổ quốc trong tim
 Tin Y tế
Tin Y tế
Đáp ứng y tế phục vụ Chương trình nghệ thuật “Tổ quốc trong tim”
 Tin Y tế
Tin Y tế
Tăng cường công tác truyền thông trong lĩnh vực y tế
 Tin Y tế
Tin Y tế
Hoàn thiện thể chế, chính sách theo mô hình chính quyền 2 cấp
 Tin Y tế
Tin Y tế
Nhận biết và đề phòng bệnh liên cầu lợn ở người
 Tin Y tế
Tin Y tế
Các ca nhiễm bệnh liên cầu lợn đang tăng nhanh ở nhiều địa phương
 Tin Y tế
Tin Y tế
















